![]()
La Société Française d’Ecologie (SFE) vous propose ce regard d’étudiants, en 4e année à l’Institut Polytechnique LaSalle Beauvais, sur la biodiversité des sols.
MERCI DE PARTICIPER à ces regards et débats sur la biodiversité en postant vos commentaires et questions sur les forums de discussion qui suivent les articles; les auteurs vous répondront.
1000 Kilogrammes sous vos pieds…
par les étudiants de la promotion 155 en quatrième année du cycle ingénieur de l’Institut Polytechnique LaSalle Beauvais,
parcours Agroécologie, Sols, Eaux et Territoires (ASET)
Encadrés par Anne-Maïmiti Mercadal, Michel-Pierre Faucon et David Houben, enseignants chercheurs de l’unité de recherche HydrISE (UP 2012.10.102), Institut Polytechnique LaSalle Beauvais
D’après des chercheurs, il s’agit de la biomasse moyenne de lombrics par hectare en France (Rovillé et Lavelle, 2015). Mais ce n’est pas tout : le sol abrite de nombreuses autres espèces. Elles s’épanouissent dans le sol et rendent de nombreux services aux écosystèmes et à travers eux, aux hommes. Par exemple, elles garantissent la fertilité du sol en participant à la mise en place de sa structure et au cycle des nutriments minéraux, ce qui est crucial pour l’agriculture. Cependant, les agronomes et les agriculteurs observent depuis une vingtaine d’années une croissance très faible voire nulle des rendements agricoles (Calderini et Slafer, 1998 ; Brison et al., 2010). Ce phénomène est expliqué par des raisons multiples et suggère que l’intensification de l’agriculture a atteint ses limites. Cette intensification est par ailleurs une des causes principales d’érosion de la biodiversité (MEA, 2005). Voyant leur abondance et leur diversité diminuer, les communautés vivantes du sol ont cessé de jouer convenablement leur rôle dans l’écosystème. Ces observations ont permis de mettre en lumière leur rôle ainsi que la nécessité de les étudier et de les protéger. Cette nécessité s’insère dans une volonté de préserver leurs rôles dans les écosystèmes mais aussi dans la mise en place de nouvelles pratiques durables, répondant aux enjeux futurs de l’agriculture comme l’emploi réduit des pesticides, la diminution du travail du sol et de la consommation des énergies fossiles (INRA, 2008).
Qui sont les êtres vivants du sol ?
Tout ce beau monde est contenu dans quatre groupes fonctionnels (Lavelle, 1998, Barot et Dubs 2012). Chaque groupe est composé d’une multitude d’espèces, qui partagent les mêmes fonctions et interactions. Les transformateurs de litière sont les premiers décomposeurs de la matière organique qui est, ensuite, minéralisée par les microorganismes. Les ingénieurs du sol, quant à eux, permettent de structurer le sol en améliorant l’infiltration de l’eau, de l’air et le développement des racines (Figure 1). Les microprédateurs se nourrissent des microorganismes.
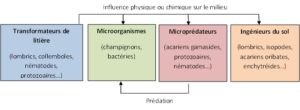
Figure 1 : Relations entre les principaux groupes fonctionnels de la biodiversité du sol
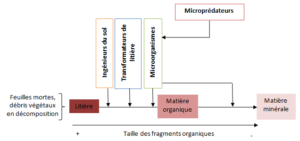
Figure 2 : Influence de la biodiversité du sol sur la transformation de la litière et la minéralisation de la matière organique du sol
Le sol, une véritable métropole
Les communautés vivantes dépendent des paramètres physico-chimiques du sol : son pH, son humidité, sa texture et sa structure, sa teneur en matière organique, sa conductivité électrique, sa capacité d’échange cationique (CEC), sa fraction minérale, etc. (Gobat et Matthey, 2010). Tous ces paramètres conditionnent le maintien des chaînes trophiques et nous renseignent sur les conditions propices au développement de certains groupes fonctionnels d’un sol, comme les microorganismes. A contrario, d’autres groupes fonctionnels sont capables de modifier ces caractéristiques. C’est le cas des ingénieurs du sol qui, grâce à la construction de galeries et de monticules, influencent la disponibilité des ressources (Jouquet et al., 2006).
Les pratiques culturales, un chantier permanent
Et la charrue dans tout ça ?
L’arsenal des techniques de travail du sol impacte la diversité fonctionnelle et spécifique de ses communautés, en affectant directement les populations et en modifiant indirectement les paramètres physico-chimiques de leur habitat (Figure 2 ; Marasas, 2001). Les techniques de travail du sol sont le labour, pouvant atteindre 40 cm de profondeur, et les techniques de non-labour, dites Techniques Culturales Simplifiées (TCS). Ces dernières peuvent être classées en trois rubriques (Smith et al., 2014) :
- travail du sol profond, en dessous de 15 cm ;
- travail du sol superficiel, au-dessus de 15 cm ;
- semis direct où le sol n’est pas travaillé du tout.
Le labour est plutôt défavorable aux organismes du sol. En effet, il détruit les galeries creusées par les habitants du sol comme les vers de terre et rend donc difficile la circulation de l’eau, des gaz et des nutriments dans le sol (Van Capelle et al., 2012). Il peut induire une compaction du sol ainsi qu’une réduction de la quantité de matière organique dans le sol, favorable à l’adsorption des éléments nutritifs (Rosell, 1993 In : Crovetto et Lamarca, 2008). De plus, lorsque la terre est régulièrement labourée, une couche compacte de terre, appelée semelle de labour, se forme à la profondeur à laquelle est effectuée le labour. Cette semelle crée une couche imperméable, qui forme un obstacle au déplacement de la faune et aux échanges gazeux. Les TCS et le semis direct sont plus favorables à la biodiversité du sol. Ils permettent l’accumulation de débris végétaux en surface et favorisent ainsi le développement des communautés de détritivores (Jeffery, 2007). Ces débris végétaux conduisent à la formation d’une litière qui participe à la naissance d’un horizon organique en surface. Cet horizon forme un habitat favorable aux communautés vivantes du sol (comme refuge et source de nourriture), en tamponnant les variations de température, en stabilisant la structure du sol et en améliorant la rétention en eau et éléments nutritifs (Kladivko, 2001).
La succession de couverts, à table !
Le type, la succession et l’association de cultures ainsi que les couverts intermédiaires et permanents influencent les communautés des organismes du sol (Figure 2 ; Rice et Gowda, 2011). Ceux-ci diminuent l’érosion éolienne et hydraulique du sol en améliorant sa stabilité structurale (Fattet et al., 2011), et permettent de conserver un sol humide plus longtemps (Huang et al., 2014). Dans ces conditions, la minéralisation de la matière organique est favorisée (Zibliske et Makus, 2009).
Les résidus des couverts végétaux sont une bonne source de carbone pour le sol. Ils contribuent à l’augmentation de son taux de matière organique (Meng et al., 2005). Cette dernière renferme l’azote tant convoité par les cultures pour leur croissance. Les plantes cultivées influencent le développement de la biodiversité du sol par l’intermédiaire de leurs racines et de leurs résidus aériens (Marschner et al., 2001 ; Nannipieri et al., 2003, Grayston et al., 1998 ; Dennis et al., 2010). La quantité et la qualité de la litière sont des facteurs du développement des communautés microbiennes et de la faune du sol.
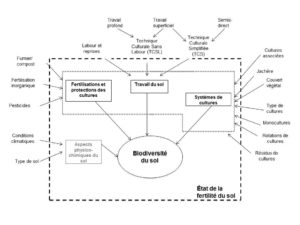
Figure 3 : Résumé des mécanismes par lesquels la biodiversité du sol est influencée par le système de culture.
Zoom sur notre projet
Les résultats présentés ci-après sont le fruit d’une étude originale menée sur une année par 24 étudiants ingénieurs spécialisés dans le parcours « Agroécologie, Sols, Eaux et Territoires » et encadrés par leurs professeurs. Le sujet de ce projet est l’analyse de l’effet des pratiques agricoles et des systèmes de culture sur la biodiversité du sol. Son originalité repose sur le fait que nous avons étudié cet effet de façon combinée et à l’échelle “grandeur nature” d’une exploitation agricole. De nombreux articles relatent l’étude de l’effet des pratiques agricoles sur les organismes du sol ; cependant, ces études sont menées en conditions contrôlées, c’est-à-dire en laboratoire (pots) ou en champs, mais sur de petites surfaces (micro parcelles, placettes). Pour notre projet, nous avons réalisés des prélèvements sur les parcelles de la ferme de l’Institut Polytechnique LaSalle Beauvais, en Picardie (Figure 4).
Figure 4 : Situation de Beauvais, en Picardie
Deux grandes problématiques ont été retenues :
- L’effet des systèmes de culture sur la biodiversité du sol,
- L’effet du travail du sol sur sa biodiversité.
Pour aborder ces deux problématiques, un dispositif basé sur le suivi de 14 parcelles (4 quadrats/parcelle) a été mis en place sur la ferme du Bois de l’Institut LaSalle (Figure 6). Le large panel de techniques culturales développées sur cette exploitation offre un cadre unique pour une telle étude, qui se veut représentative de la région. En effet, nos travaux combinent et testent simultanément in situ l’influence de ces différents systèmes culturaux sur la biodiversité du sol, et ce dans les mêmes conditions climatiques. Nous avons étudié la structure des communautés lombriciennes et la respiration du sol. Cette dernière est une résultante de l’activité biologique (par la dégradation de la matière organique) et de la respiration racinaire. Le groupe des lombrics est, quant à lui, accessible à l’observation et sensible aux pratiques culturales.
Ainsi, pour étudier la pression des pratiques agricoles sur les communautés lombriciennes, nous avons effectué dans chaque parcelle sélectionnée quatre prélèvements de lombrics (Figures 5 et 6), pour lesquels le nombre total de lombrics, et le nombre d’espèces différentes ont été déterminés. Parallèlement, des mesures de respiration du sol ont été réalisées (Figure 5 et 6).

Figure 5 : (A) Analyse de la composition d’un prélèvement de lombrics et (B) mesure de respiration du sol en plein champ
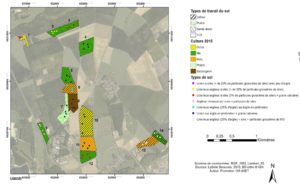
Figure 6: Carte de la position des parcelles sélectionnées sur le parcellaire de la ferme du Bois pour l’étude et précision des différentes techniques de travail du sol, des différentes cultures et des différents types de sols présents sur ces 14 parcelles (ASET 155, 2015)
Des résultats en abondance !
Le fait que le projet étudie in situ l’influence de ces différents systèmes culturaux sur la biodiversité du sol nous permet de réaliser des analyses statistiques multivariées, prenant en compte de nombreux facteurs. Ainsi, nous avons pu tester (1) l’impact des différentes pratiques de travail du sol,(2) l’impact des conditions physico-chimiques du sol (type de sol, pH etc.) (3) l’impact des systèmes de culture sur la biodiversité du sol.
Notre étude et les tests statistiques associés (plus de 155 tests statistiques réalisés !) mettent en avant deux facteurs clés influençant les lombrics et la respiration du sol : le type de sol et le travail du sol. Concernant le type de sol, un pH neutre et une texture limono-argileuse, sont plutôt favorables aux vers de terre. Le travail du sol est une des pratiques qui a le plus de répercussions sur les communautés de lombrics. En effet, nous avons mis en évidence un effet significatif du travail du sol sur l’abondance totale des lombrics. Il y a plus de lombrics dans les parcelles en semis direct (92 ± 43 individus par m²) qu’en labour (38 ± 9 individus par m²) ce qui vient confirmer les travaux de Chan (2001). Toutefois, notons que la parcelle en semis direct sur laquelle le plus grand nombre de vers de terre a été capturé (201 ± 31 individus par m²), est la seule ayant reçu un couvert intermédiaire à base de lentilles, vesce, phacélie, pois et seigle, ce qui pourrait également avoir une influence. Ces résultats concernent en particulier le groupe fonctionnel des anéciques (représenté uniquement par l’espèce Lumbricus terrestris) qui se classe en première position sur l’ensemble de nos échantillons (avec plus de 70 % des individus piégés). Le groupe fonctionnel des endogés, à l’inverse, tend à être favorisé par le labour, ce qui vient confirmer les travaux de Berner et al. (2008). En effet, le labour leur permet de redistribuer les nutriments présents en surface, ce qui permet à ces vers de terre vivant entre 5 et 40 cm de profondeur (Institut de recherche de l’agriculture biologique, 2013), d’y avoir accès. Enfin, du fait de la faible représentation du groupe fonctionnel des épigés en milieu agricole, ce groupe n’a pas été pris en compte dans notre étude.
Par rapport au semis direct, nos relevés de respiration soulignent l’effet négatif du labour sur les microorganismes du sol. Il est probable que ce phénomène s’explique par le fait que, suite à un labour, le sol se compacte de nouveau et les résidus enfouis se retrouvent alors en conditions anaérobies. Leur dégradation est ralentie, elle induit donc une diminution de l’activité des microorganismes décomposeurs. Un effet positif du labour sur la respiration du sol peut cependant être observé, mais à court terme (seulement quelques jours après l’opération) car en retournant la terre, il permet son aération (Oorts et al., 2007).
Parmi l’ensemble des facteurs étudiés, le travail du sol semble avoir le plus d’influence sur les vers de terre et sur la vie du sol (respiration du sol). Mais l’importance de son effet est variable et dépend notamment d’autres facteurs, comme la succession des couverts et le type de culture. Ces derniers affectent les organismes du sol, mais dans une moindre mesure.
Conclusion
La biodiversité du sol est de mieux en mieux connue, mais les connaissances acquises à ce jour peuvent paraitre minimes lorsque l’on considère cet énorme réservoir de biodiversité sous nos pieds. Néanmoins, la volonté d’une compréhension globale des systèmes agricoles par divers acteurs suggère une mobilisation future dans ce sens. Les agro-systèmes étant complexes, d’autres études doivent être réalisées. Par exemple, quels sont les impacts de la fertilisation sur la biodiversité du sol ? Quel rôle jouent les organismes du sol dans la dégradation des pesticides présents dans les sols ? Beaucoup d’autres questions restent encore sans réponse et chercher à y répondre nous permettra à l’avenir d’adapter nos pratiques agricoles et de préserver durablement nos sols..
Glossaire
Anéciques : catégorie de vers de terre bruns de grande taille se nourrissant de matière organique à la surface et vivant dans des galeries verticales pouvant atteindre 3m de profondeur. Avec les lombrics endogés, ils forment les vers laboureurs.
Biodiversité : Terme qui désigne la diversité du monde vivant à tous les niveaux : diversité des milieux (écosystèmes), diversité des espèces, diversité génétique au sein d’une même espèce.
Capacité d’Échange Cationique (CEC) : somme des cations (potassium, magnésium, calcium…) que le sol peut échanger. Représente la taille du réservoir permettant de stocker de manière réversible ces éléments fertilisants cationiques.
Chaîne trophique : ensemble d’organismes liés par des liens trophiques. On distingue les producteurs (plantes cultivées, par exemple), les consommateurs primaires (herbivores), les consommateurs secondaires (carnivores) et les décomposeurs (ou détritivores).
Communauté : association de populations de différentes espèces en interaction, généralement définie sur la base de leurs interactions et/ou du lieu dans lequel elles vivent.
Composés humiques : matières organiques issues de la décomposition des végétaux incorporées dans le sol.
Conductivité électrique : aptitude d’un matériau ou d’une solution à laisser les charges électriques se déplacer librement, autrement dit à permettre le passage du courant électrique.
Diversité fonctionnelle : variété des regroupements des espèces sur la base de similarité des fonctions qu’elles occupent dans l’écosystème.
Diversité spécifique : diversité d’espèces dans un espace donné.
Endogés : catégorie de vers de terre apigmentés, de taille variable se nourrissant de la matière organique du sol et vivant dans premiers centimètres du sol, dans lequel ils construisent des réseaux de galeries subhorizontales. Ils font partie, avec les lombrics anéciques, des lombrics laboureurs.
Épigés : catégorie de vers rougeâtres et de petite taille, se nourrissant uniquement de la matière organique se décomposant dans la litière. Ils sont des vers digesteurs.
Fraction minérale : proportion des éléments minéraux du sol issu de la dégradation physique puis chimique de la roche mère (sables, limons, argiles, silicates, carbonates etc.).
Groupe fonctionnel : regroupement d’espèces en référence aux fonctions qu’elles occupent dans l’écosystème.
Horizon : couche de sol homogène et parallèle à la surface, définie en fonction de son épaisseur, de sa composition granulométrique (argiles, limons, sables), de son degré d’altération de la roche-mère, de son acidité.
Minéralisation : Processus de libération des nutriments minéraux de la forme organique vers une forme minérale assimilable par les racines.
Population : ensemble d’individus appartenant à la même espèce, présents simultanément dans un même site géographique.
Richesse spécifique : nombre d’espèces (faunistiques ou floristiques) présentes dans un espace donné.
Structure du sol : mode d’organisation en agrégats de différentes tailles des différentes particules de sable, limon et argile entre elles.
Texture du sol : indique les proportions relatives, dans le sol, de particules de dimensions variées (sable, limon ou argile).
Liste des références bibliographiques
Barot, S. Dubs F, 2012 Regard sur la Biodiversité 28, Les écosystèmes du sol, https://sfecologie.org/regard/r28-sols-barot-et-dubs/
Berner, A., Hildermann, I., Fließbach, A., Pfiffner, L., Niggli, U., etMäder, P., 2008. Crop yield and soil fertility response to reduced tillage under organic management. Soil and Tillage Research, volume 101, n° 1–2. p. 89-96
Brisson, N., Gate, P., Gouache, D., Charmet, G., Oury, F.-X., et Huard, F., 2010. Why are wheat yields stagnating in Europe? A comprehensive data analysis for France. Field Crops Research, volume 119, n° 1. p. 201-212
Calderini, D.F., et Slafer, G.A., 1998. Changes in yield and yield stability in wheat during the 20th century. Field Crops Research, volume 57, n° 3. p. 335–347
Van Capelle, C., Schrader, S., et Brunotte, J., 2012. Tillage-induced changes in the functional diversity of soil biota – A review with a focus on German data. European Journal of Soil Biology, volume 50, p. 165-181
Chan, K.Y., 2001. An overview of some tillage impacts on earthworm population abundance and diversity — implications for functioning in soils. Soil and Tillage Research, volume 57, n° 4. p. 179-191
CNRS/sagascience – Le ver de terre, star du sol, [en ligne]. Date de consultation : 13/02/2016. Disponible sur : <http://www.cnrs.fr/cw/dossiers/dosbiodiv/index.php?pid=decouv_chapC_p5&zoom_id=zoom_c1_8>
Crovetto Lamarca, C., 2008. Les fondements d’une agriculture durable II : nourrir le sol, un enjeu mondial. Panam ; [Teknea], Villemur-sur-Tarn (Domaine de Carles, route de Villebrumier, 31340); Paris : ISBN 2877170764 9782877170765.
Dennis, P.G., Miller, A.J., et Hirsch, P.R., 2010. Are root exudates more important than other sources of rhizodeposits in structuring rhizosphere bacterial communities?: Root exudates and rhizosphere bacteria. FEMS MicrobiologyEcology, volume 72, n° 3. p. 313-327
Fattet, M., Fu, Y., Ghestem, M., Ma, W., Foulonneau, M., Nespoulous, J., Le Bissonnais, Y., et Stokes, A., 2011. Effects of vegetation type on soil resistance to erosion: Relationship between aggregate stability and shear strength. CATENA, volume 87, n° 1. p. 60-69
Gobat, J.M., et Matthey, W., 2010. Le sol vivant: bases de pédologie, biologie des sols. PPUR Presses Polytechniques, : 817 p.
Grayston, S.J., Wang, S., Campbell, C.D., et Edwards, A.C., 1998. Selective influence of plant species on microbial diversity in the rhizosphere. Soil Biology and Biochemistry, volume 30, n° 3. p. 369-378
Huang, J., Wang, J., Zhao, X., Wu, P., Qi, Z., et Li, H., 2014. Effects of permanent ground cover on soil moisture in jujube orchards under sloping ground: A simulation study. Agricultural Water Management, volume 138, p. 68-77
Jeffery, S., 2007. The microbiology of arable soil surfaces.CranfieldUniversity. 1229 p.
Jouquet, P., Dauber, J., Lagerlöf, J., Lavelle, P., et Lepage, M., 2006. Soil invertebrates as ecosystem engineers: Intended and accidental effects on soil and feedback loops. Applied Soil Ecology, volume 32, n° 2. p. 153-164
Kladivko, E.J., 2001. Tillage systems and soil ecology.Soil and Tillage Research, volume 61, n° 1–2. p. 61-76
Lavelle, P., 1988. Earthworm activities and the soil system.Biology and Fertility of Soils, volume 6, n° 3. p. 237-251
Institut national de la recherche agronomique, 2009. Agriculture et biodiversité: Valoriser les synergies. Éditions Quae
Institut de recherche de l’agriculture biologique, FiBL, 2013. Vers de terre – Architectes des sols fertiles [en ligne]. Disponible sous <https://www.fibl.org/fileadmin/documents/shop/1619-vers-de-terre.pdf>
Marasas, M.E., Sarandón, S.J., et Cicchino, A.C., 2001. Changes in soil arthropod functional group in a wheat crop under conventional and no tillage systems in Argentina. Applied Soil Ecology, volume 18, n° 1. p. 61-68
Marschner, P., Yang, C.-H., Lieberei, R., et Crowley, D.E., 2001. Soil and plant specific effects on bacterial community composition in the rhizosphere. Soil Biology and Biochemistry, volume 33, n° 11. p. 1437–1445
Millennium Ecosystem Assessment. http://www.millenniumassessment.org/fr/
Meng, L., Ding, W., etCai, Z., 2005. Long-term application of organic manure and nitrogen fertilizer on N2O emissions, soil quality and crop production in a sandy loam soil. Soil Biology and Biochemistry, volume 37, n° 11. p. 2037-2045
Nannipieri, P., Ascher, J., Ceccherini, M.T., Landi, L., Pietramellara, G., et Renella, G., 2003. Microbial diversity and soil functions. European Journal of Soil Science, volume 54, p. 655-670
Oorts, K., Merckx, R., Gréhan, E., Labreuche, J., et Nicolardot, B., 2007. Determinants of annual fluxes of CO2 and N2O in long-term no-tillage and conventional tillage systems in northern France.Soil and Tillage Research, volume 95, n° 1–2. p. 133-148
Rice, W.C., et Gowda, P.H., 2011. Influence of geographical location, crop type and crop residue cover on bacterial and fungal community structures. Geoderma, volume 160, n° 3–4. p. 271-280
Rovillé, M., et Lavelle, P., 2015. Le ver de terre, star du sol, http://www.cnrs.fr/cw/dossiers/dosbiodiv/index.php?pid=decouv_chapC_p5&zoom_id=zoom_c1_8
Smith, E. K., Misiewicz, P. A., Girardello, V., Arslan, S., Chaney, K., White, D. R., & Godwin, R. J. (2014). Effects of traffic and tillage on crop yield (winter wheat, Triticum aestivum L.) and the physical properties of a sandy loam soil. ASABE Paper No. 141912652. St. Joseph, Mich.: ASABE.
Zibilske, L.M., et Makus, D.J., 2009. Black oat cover crop management effects on soil temperature and biological properties on a Mollisol in Texas, USA. Geoderma, volume 149, n° 3–4. p. 379-385
Rice, W.C., et Gowda, P.H., 2011. Influence of geographical location, crop type and crop residue cover on bacterial and fungal community structures. Geoderma, volume 160, n° 3–4. p. 271-280
Zibilske, L.M., et Makus, D.J., 2009. Black oat cover crop management effects on soil temperature and biological properties on a Mollisol in Texas, USA. Geoderma, volume 149, n° 3–4. p. 379-385
Le texte de ce regard est sous licence Creative Commons by-sa 4.0.
Edition et mise en ligne : S. Barot
——


Bravo!
« Le sol vivant » est ces derniers temps très en vogue, notamment dans les média!
et Ingénieurs du sol et ingénieurs de l’Institut Polytechnique sont parfaitement en phase!
Commentaires sur le fond suivront…
PS : la figure 1 n’apparait pas.
Merci Thierry, j’ai corrigé le problème pour la figure.
Sébastien