La Société Française d’Ecologie et d’Evolution (SFE2) vous propose ce regard de Christian Peeters et Nathan Cyrille, respectivement Directeur de Recherches en écologie et étudiant en 2e année de Master d’écologie, sur le comportement et l’écologie des fourmis tunnelières.
MERCI DE PARTICIPER à ces regards et débats sur la biodiversité en postant vos commentaires et questions sur les forums de discussion qui suivent les articles; les auteurs vous répondront.
———-
Melissotarsus, fourmis tunnelières
et éleveuses de cochenilles
par
Christian Peeters(1) et Nathan Cyrille(2)
(1) : Directeur de Recherches CNRS au laboratoire IEES, Paris,
(2) : Stagiaire de M2 à l’IEES
Article édité par Sébastien Barot
——-
Mots clés : Fourmis, Melissotarsus, écologie, comportement, adaptation, évolution, mutualisme, insectes sociaux.
——–
- (Introduction)
- Melissotarsus, une fourmi éleveuse de diaspines
- Melissotarsus, une fourmi tisseuse et maçonne
- Melissotarsus et diaspines, une relation de mutualisme ?
- Bibliographie
- Regards connexes
- Forum de discussion sur ce regard
——
(Introduction)
Si des milliers d’espèces de fourmis sont arboricoles, peu d’entre elles sont capables de construire des tunnels dans du bois vivant. Parmi celles-ci, les minuscules fourmis (2,5 mm) du genre Melissotarsus (sous-famille Myrmicinae), présentes au sein de nombreuses essences d’arbres sur tout le continent africain, disposent de remarquables adaptations squeleto-musculaires leur permettant d’être parfaitement adaptées à la vie cryptique qu’elles mènent sous l’écorce (cliquer ici pour manipuler une ouvrière en 3D). Par exemple, pour creuser leur réseau de galeries dans le bois, les ouvrières ont non seulement une tête fortement élargie avec plus de la moitié occupée par les muscles des mandibules, mais aussi une couche de zinc protégeant l’extrémité des mandibules (Khalife et al., 2018). De plus, les pattes médianes de Melissotarsus sont orientées latéralement, adaptation qui leur confère un meilleur appui sur les parois des galeries et leur permet de mieux se déplacer au sein des tunnels (Khalife et al., 2018). Cette adaptation détonante est tellement prononcée que cette fourmi est incapable de marcher sur une surface plane à l’extérieur des galeries ; c’est d’ailleurs pourquoi elle avait été nommée M. titubans après sa découverte en 1972 par Bernadette Delage-Darchen.
Melissotarsus, une fourmi éleveuse de diaspines
Mais alors, si ces fourmis qui mènent une vie cachée sous l’écorce sont incapables de se déplacer à l’extérieur de leur arbre hôte, comment font-elles pour se nourrir ? C’est là qu’intervient le second protagoniste de cette passionnante histoire naturelle. En effet, les fourmis vivent en présence de cochenilles diaspines (Morganella conspicua) (Fig. 1). La famille des Diaspididae (2700 espèces) est caractérisée par 1) l’absence de sécrétions de miellat (Foldi, 1990) et 2) la formation d’un bouclier protecteur chez les femelles. De nombreux cas de relation fourmis-cochenilles ont déjà été mis en lumière, mais celui-ci est le premier faisant intervenir une cochenille n’excrétant pas de miellat, ce qui rend la nature de l’alimentation obtenue par Melissotarsus incertaine. Alors que les diaspines mâles sont des insectes ailés destinés uniquement à la dispersion et la reproduction, les diaspines femelles sont aptères et se fixent sur le bois via leur stylet. Ce stylet leur permet de se nourrir des cellules de l’arbre (parenchyme), après émission d’une salive composée d’enzymes (Foldi, 1990). Les diaspines femelles passent par trois stades successifs au cours de leur développement : le premier stade où l’individu nommé « crawler » est mobile, et les deux stades suivants marqués par la fixation définitive de la diaspine femelle via l’ancrage de son stylet, la perte des pattes et antennes, et la formation du bouclier en cire. Chose remarquable, ce bouclier est absent dans les nids de fourmis. Par ailleurs, alors que les fourmis Melissotarsus sont toujours trouvées en présence de diaspines, la réciprocité n’est pas de mise. En effet, ces mêmes cochenilles peuvent également être observées en surface de l’écorce, sans les fourmis et entourées du bouclier emblématique de la famille des diaspines !

Fig. 1. Ouvrières Melissotarsus entourées d’une multitude de cochenilles diaspines. A noter l’absence de boucliers de cire qui sont pourtant la caractéristique des diaspines. (cliché C. Peeters)

Fig.2 Arbre Leucospermum praemorsum habité par Melissotarsus en Afrique du Sud. Une portion de l’écorce a été ouverte pour révéler le réseau de tunnels ; ailleurs, les toits de soie et sciure sont visibles. (cliché C. Peeters)
Melissotarsus, une fourmi tisseuse et maçonne
L’observation du comportement de Melissotarsus est problématique. Bien que des nids dans des branches intactes peuvent être étudiés au laboratoire, ceci requiert au préalable d’ouvrir les galeries avec un couteau (Fig.2). Or, cela entraîne une perturbation immédiate de la colonie ; les fourmis mettent en parenthèse leurs activités du moment pour combler les brèches aussi vite que possible. Melissotarsus ne possède aucun attribut physique lui permettant de se défendre contre les prédateurs (principalement les nombreuses autres fourmis prédatrices arboricoles) ; en plus d’une marche chancelante, les ouvrières ont en effet perdu l’aiguillon ! Leur unique chance de subsister est donc de garder leurs galeries étanches au monde extérieur. Pour combler les brèches, les individus adultes de Melissotarsus ont évolué la capacité à produire la soie, une adaptation unique chez les fourmis (Fig.3) ! Les adultes présentent en effet des glandes à soie dans la partie ventrale de la tête, ainsi que des poils aux extrémités des pattes antérieures (ici) leur permettant de filer cette soie.

Fig. 3. Suivi temporel (en minutes) du comblement d’une brèche avec de la soie. Une ouvrière commence par déposer un épais fil composé de jusqu’à 5 filaments qui adhèrent entre eux, mettant en jeu tout autant de glandes à soie. Les poils des pattes antérieures viennent au contact de ces glandes et permettent le filage en un fil unique. L’ouvrière dépose ce fil à l’aide des deux pattes antérieures sur le pourtour de la brèche. L’ouvrière s’en va ensuite puis revient avec un amas de petits morceaux de bois dans ses mandibules. Elle passe alors l’une de ses pattes antérieures au niveau des glandes à soie. Tout en tirant des filaments dans son mouvement retour, les poils rentrent en contact avec l’amas et les filaments de soie y adhèrent. Ensuite, la fourmi emmaillote de soie l’amas, si bien que ce dernier, outre son rôle structurel, devient à son tour le support de fixation pour d’autres morceaux. Une fois le comblement bien avancé au niveau du pourtour de la brèche, l’ouvrière entreprend l’élaboration d’un maillage de soie en son centre, avec des fils et filaments qui se ramifient les uns avec les autres pour former un véritable canevas de soie. Par la suite, l’ouvrière pourra déposer directement du bois sur ce maillage, et finira par combler entièrement la brèche. (cliché C. Peeters)
Melissotarsus et diaspines, une relation de mutualisme ?
Alors qu’il n’est pas aisé d’observer les fourmis Melissotarsus au sein des galeries, il n’est pas non plus possible d’élever les fourmis hors des branches, sans les diaspines. Nous avons donc dû suivre une approche déductive via l’étude des adaptations morphologiques (par micro-tomographie, histologie et microscopie à balayage) qui permettent des prédictions fiables sur leur comportement. Par exemple, les ouvrières Melissotarsus ont une énorme glande labiale à l’arrière du thorax (Fig.4), ce qui n’est pas le cas chez les autres fourmis. Cette expansion est possible suite à la réduction extrême des muscles du thorax qui bougent l’abdomen, conséquence de la perte de l’aiguillon (elle-même probablement la conséquence de l’abandon de la capacité à marcher hors des galeries !).
Cette glande est appelée « labiale » car elle déverse son contenu près de la bouche, ce qui laisse imaginer une pré-digestion avec des enzymes encore inconnues. Ainsi, en complément de la digestion dans l’estomac au niveau de l’abdomen, l’importante taille de la glande labiale suggère l’implication d’autres enzymes digestives pour permettre aux fourmis de s’alimenter. Les cochenilles diaspines secrètent en permanence des composés protéiques et cireux, normalement utilisés pour la confection du bouclier, et notre hypothèse est que les fourmis se nourrissent de ces exsudats, ainsi que des adultes vieillissants.
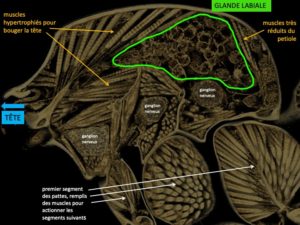
Fig. 4. Coupe tomographique à travers le thorax d’une ouvrière Melissotarsus, montrant la taille de la glande labiale sécrétrice d’enzymes déversées près de la bouche. (clichéC. Peeters)
Dans ce mutualisme, les diaspines semblent donc être utilisées comme un outil pour extraire les nutriments de l’arbre hôte. En échange, les diaspines tirent bénéfice des adaptations de Melissotarsus pour accéder aux cellules végétales et obtenir protection au sein des galeries (si bien que leur bouclier ne leur est dès lors plus nécessaire). Il est par ailleurs très probable qu’une minorité de crawlers, le seul stade de développement où les diaspines femelles sont capables de se déplacer, puissent s’échapper du nid via de petites brèches, avant de mener une vie émancipée de toute fourmi ; ceci expliquerait l’impossibilité de modifications physiologiques chez les diaspines inféodées aux fourmis, empêchant une vie autonome à l’extérieur.
A l’avenir, des recherches sur la manière dont une reine ailée forme une nouvelle colonie et enrôle des diaspines devront être menées ; cela permettra de savoir comment la relation entre ces deux protagonistes s’initie. De plus, il serait important de s’interroger sur le troisième acteur de cette étude : l’arbre hôte. Ce dernier tire-t-il un quelconque avantage de la relation diaspine-fourmi ou bien en ressort-il totalement perdant ? Compte tenu de la grande diversité des arbres hôtes (20 familles botaniques concernées), trouver un pattern commun constitue un défi.
Bien qu’elle conserve encore quelques secrets, une chose est sûre : la minuscule Melissotarsus arbore une extrême originalité et un caractère attachant indéniable !
Bibliographie
Delage-Darchen B. 1972. Une Fourmi de Côte-d’Ivoire : Melissotarsus titubans Del., n. sp. Insectes Sociaux 19:213.
Foldi I. 1990. The scale cover. In: Rosen D, ed. Armored scale insects: their biology, natural enemies and control. Vol. 4A. Amsterdam: Elsevier, pp. 43-54.
Khalife A, Keller R, Billen J, Hita Garcia F, Economo E & Peeters C. 2018. Skeletomuscular adaptations of head and legs of Melissotarsus ants for tunneling through living wood. Frontiers in Zoology, 15:30.
Peeters C, Foldi I, Matile-Ferrero D & Fisher BL. 2017. A mutualism without honeydew: what benefits for Melissotarsus emeryi ants and armoured scale insects (Diaspididae)? PeerJ 5:e3599
Mony R, Kenne , Orivel, J & Dejean A. 2002. Biology and ecology of pest ants of the genus Melissotarsus (Formicidae: Myrmicinae), with special reference to tropical fruit tree attacks. Sociobiology, 40:645-654.
Regards connexes
(A compléter, ou supprimer…)
—-
Article édité et mis en ligne par Sébastien Barot.
——
Forum de discussion sur ce regard


Commentaires récents